12日、18日に薬事審議会要指導・一般用医薬品部会の開催が発表され、シアリス(タダラフィル)の要指導医薬品への指定の要否及び製造販売承認の可否について非公開で審議されることが発表されています。
【厚労省 2025.09.12】
薬事審議会 要指導・一般用医薬品部会を開催します
https://www.mhlw.go.jp/stf/newpage_63362.html
議題(非公開案件):
シアリスの要指導医薬品への指定の要否及び製造販売承認の可否について
https://www.mhlw.go.jp/content/11121000/001560974.pdf
申請はエスエス製薬で、5月23日の「医療用から要指導・一般用への転用に関する評価検討会議」への出席に際して、承認申請を行っていることを明らかにしています
エスエス製薬の「医療用から要指導・一般用への転用に関する評価検討会議」出席について
(エスエス製薬2025.05.23)
https://www.ssp.co.jp/news/2025/20250523/
承認申請から、要指導・一般用医薬品部会での承認の可否審議までに異例の速さと思うかもしれませんが、これは規制改革実施計画(令和6年6月21日閣議決定)での「厚生労働省は、スイッチOTC化の承認申請から承認の可否判断までの総期間を1年以内(令和5年以前に申請があったものは令和6年末まで。以下同じ。)に設定する」を受けてスピードアップが図られたもので、巷でささやかれている特別扱いをされたものではありません。
TOPICS 2025.05.24 で紹介しましたが、スイッチOTC化に向けての見解や論点は、医療用から要指導・一般用への転用に関する評価検討会議で明らかになっています。
スイッチOTC医薬品の候補成分に関する見解
https://www.mhlw.go.jp/content/11121000/001492239.pdf
日本泌尿器学会:賛成
日本臨床泌尿器学会:賛成
日本性機能学会:賛成
日本臨床内科医会:反対
日本OTC医薬品協会:賛成
議事録(→リンク)を見ても、参考人(泌尿器科医師)から、オンライン診療で医師が必ずしも必要な確認をとっていない現状や個人輸入などで自己判断でたくさん服用している危険な事例があるという現状への懸念や、糖尿病や心血管障害の新たな隠れた病気の発見につながるの可能性があるとしておおむね賛成の声が多く、了承される可能性は高いと考えています。
ただ、承認の可否となると部会の委員の日医や内科医の先生方から、薬剤師が心血管リスクのチェックや受診勧奨を積極的に行えるのかどうかの指摘が行われ、個人的には差し戻しになる可能性が半分くらいあると思っています。
現在、海外のED治療薬のスイッチ状況ですが、処方箋なしで購入できる国はまだ少なく、当局が審議の末に認めていない国もあります。
1.ポーランド(シルデナフィル、2016:タダフィル、2022)
シルデナフィルは25mg/50mgが、2016年にOTC化(→Meicare.PL)、タダラフィルは2022年2月にOTC化(→Mgr.farm) 価格は結構安かった。
2.英国(シルデナフィル、2018:タダフィル、2023)
2017年3月に当局のMHRAがシルデナフィルのOTC化の方針を示し、販売方法などについて意見募集を実施、概ね賛成の意見で占められ、同年11月に再分類することを発表。
PGD(Patient Group Direction)などによる販売がすでに行われていた、偽造医薬品による健康被害から国民を守る、販売時のチェックにより、EDの原因となる脂質異常症や心臓病、糖尿病などの早期発見につながる可能性があるなどのメリットを挙げた。(→TOPICS 2017.11.29)
2023年3月にはタダラフィルの再分類を発表(→MHRA 2023.03.14)(→関連Xへの投稿)
3.アイルランド(シルデナフィル、2021:タダフィル、2023)
チェックリスト(→Viagra Connect)に沿って販売
4.ドイツ(未承認)
スイッチの申請はこれまで3度行われたが、直近の2025年1月に開催されたドイツ当局のBfArMの処方要件に関する専門家委員会でみたび却下。EDの男性が(薬局を通じて)医療を受けられるようになる可能性があるとの見解が示された一方、複数の委員から、特に若い男性は性的「パフォーマンス」に関して疑問を抱いている可能性があり、その場合、性的治療や心理的支援アプローチがより必要になるだろうと指摘がその理由。(→TOPICS 2025.04.22)
5.ノルウェー(シルデナフィル、2019:タダラフィル、2025)
処方箋医薬品販売指導制度(→ノルウェー医薬品庁)に従い、2019年より処方箋なしでの販売が可能に。6ヶ月以内にかかりつけ医による健康診断を受けることを推奨(→ノルウェー医薬品庁)。
一方で、チェックリスト(→リンク)による販売が行われるも、しっかり遵守されていないという指摘も(→Int J Pharm Pract. )。
2025年11月には、タダラフィルについても処方箋なしでの販売が可能になった(→ノルウェー医薬品庁 2025.11.18)
6.スイス(シルデナフィル、2020)
Liste B+ という、正当な理由のある例外的な場合に限り、医師の処方箋なしに患者に薬剤師が処方薬を調剤する仕組みで販売が可能に(→TOPICS 2025.05.24)
7.ニュージーランド(シルデナフィル、2014)
2013年11月のMEDSAFEの医薬品分類に関する委員会で審議も、「スクリーニングチェックツールの不備や健康リスクを申告しない生活者が潜在するとして、スイッチはすべきでない」として差し戻されたが、2014年4月の同会議で了承、同年10月に、処方せん医薬品(Schedule1)のままで、一定の条件の下であれば、処方せんなしでの販売を認めることを官報で告知。(→TOPICS 2014.10.17)
8.豪州(スイッチ未承認)
2014年に2回目のスイッチ申請も、12月にシルデナフィルが使用される病気や症状には、適切な医学的評価と診断を確実にし、根本的な原因となる健康状態の治療における医学的支援を促進するための医療介入が必要である、また相互作用への懸念があるとして再び却下したことを発表(→Xへの関連投稿)
Notice of final decisions to amend (or not amend) the current Poisons Standard
(TGA 2024.12.16)
https://www.tga.gov.au/sites/default/files/2024-12/notice-final-decisions-amend-not-amend-current-poisons-standard-june-2024.pdf
やはり、一部の国では、心血管リスクのチェックや受診勧奨を積極的に行えるのかどうかなどが懸念になっているようです。
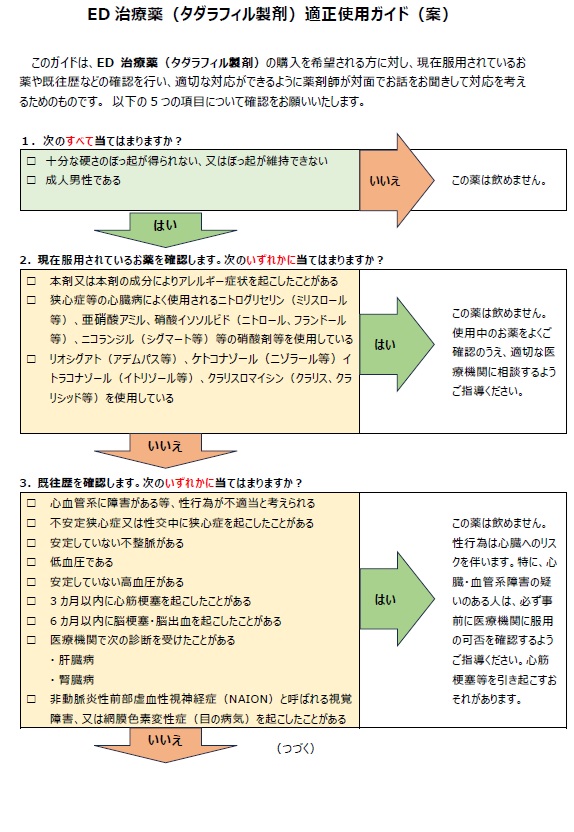
日本ではどうなるかというと、評価検討会議会議で、下記のようななチェックリスト案が示されています。(要指導・一般用医薬品部会での資料はおそらく非公開も、この案が提示される可能性大)
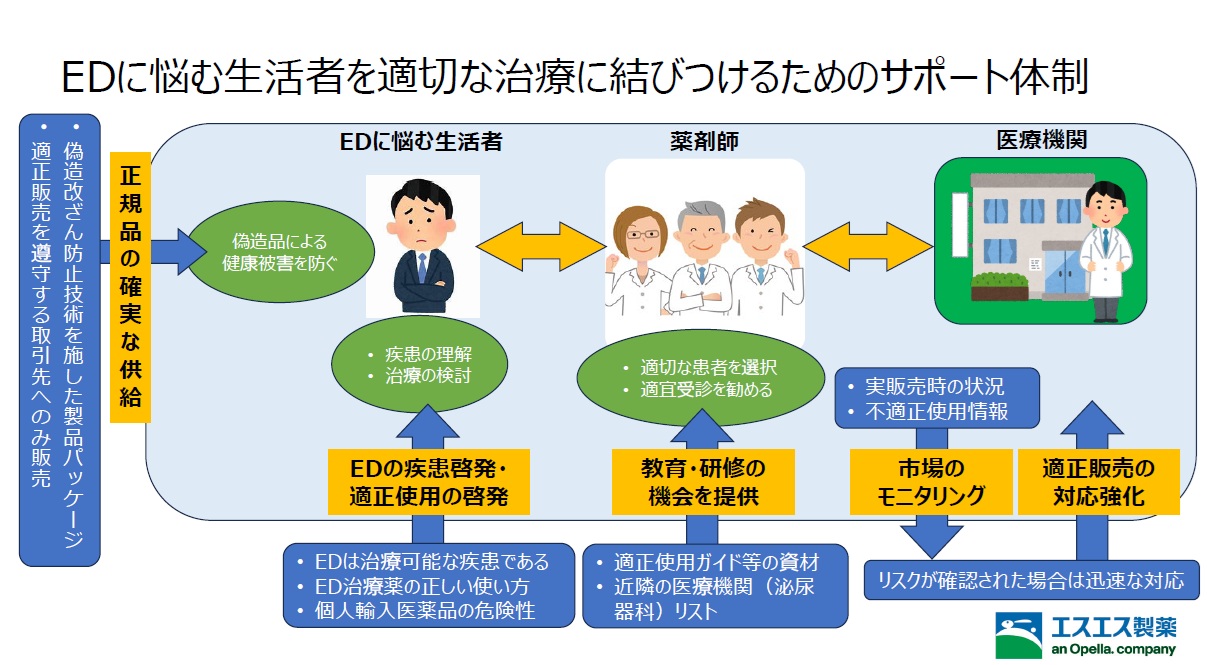
~EDに悩む多くの方々に品質の確かなED治療薬を届けたい~
(エスエス製薬)
https://www.mhlw.go.jp/content/11121000/001492511.pdf

確かにこれが確実に行われれば、安全に販売・使用が行われることでしょう。
(これだけのことが現状行われているかどうかは疑問の声も)
一方流通の問題は課題を残します。
エスエス製薬は直販メーカーであり、シアリスがスイッチされても、同社が供給するアレグラFXプレミアムや、大正製薬のアライのように、「適正価格で適正量を供給」という名の下に、当初の供給は販売力のあるドラッグ(併設店)や量販店のみとし、直接の取引がない一般の調剤主力店は取り扱えなくなる懸念があります。
(議事録から)
弊社は直販体制を取っておりまして、販売店・薬局様のほうにどれぐらい卸していて、どれぐらい注文が来てというのはきちんと把握できる状態にございますので、異常な量の発注があった場合には、これはどうしてこんなに今月は多いのですかというのを必ず確認して、何か理由が明確でなければもちろんお断りするという形を取りますので、言葉は悪いですけれども、裏の社会に流れるとか、そういうことも考えにくいと思っております。
これらを踏まえ、承認の可否がどうなるか注目です。
関連情報:TOPICS
2025.08.19 Liste B+ 医薬品は日本でいうところの零売?(スイス)
2025.05.24 ED治療薬のスイッチOTC化に向けての議論(評価検討会議・速報)
2025.05.19 EDの管理とセルフケアにおける薬剤師の役割(FIP)
2025.04.23 プライマリケアにおける薬剤師の役割を拡大するための医薬品の分類(豪・NZ)
2025.04.22 シルデナフィルのOTC化は今回も認めず(独・専門委)
2017.11.29 バイアグラの処方箋なしでの購入が可能に(英国)
2014.10.17 シルデナフィルが処方せんなしで購入可能に(NZ)
2026.02.03 01:10追記
2025年09月16日 14:48 投稿

「要指導医薬品」への指定が了承されたそうです。
非公開なので資料が出ないので、各社記事を貼っておきます
ED治療薬、国内初の市販化へ 薬剤師による対面販売
(毎日新聞 2025.09.18)
https://mainichi.jp/articles/20250918/k00/00m/040/282000c
https://news.yahoo.co.jp/articles/54c9e6dd0f62a54c40668b284b461049da70b2c1
薬機法改正でしかたないのですが、ネット購入を可にしたら転売目的の複数個購入とかどう管理するんでしょうね
さらに供給先の選別を行ったりすれば、調剤主力のところはあえて取り扱わないかも
ドラッグ併設やチェーンさんが圧倒的に優位ですね
これで、アクセス向上に果たしてつながるのか
一方、オンライン診療で稼いでいた人たちは困るだろうな
>今年成立した改正医薬品医療機器法に基づき、来年5月以降は、オンラインで薬剤師の説明を受けることで、インターネットで購入できるようになる。
ED治療薬、処方箋不要に 国内初、薬剤師の指導必要
(共同通信/東京新聞 2025.09.19)
https://www.tokyo-np.co.jp/article/436814
https://www.m3.com/news/general/1296958
2月2日に非公開で開催された要指導・一般用医薬品部会で、前回の部会で指摘された点への対応状況が説明されています。
議題
https://www.mhlw.go.jp/content/11121000/001630430.pdf
これを受け、正式承認に向けたパブリックコメントが始まっています。(3月4日まで)
【e-gov】
医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律第四条第五項第三号の規定に基づき厚生労働大臣が指定する要指導医薬品の一部を改正する告示(案)に関する御意見の募集について
https://public-comment.e-gov.go.jp/pcm/detail?CLASSNAME=PCMMSTDETAIL&id=495250400&Mode=0
https://public-comment.e-gov.go.jp/pcm/download?seqNo=0000306723
指摘事項があったのであれば、緊急避妊薬のときのようになぜ販売体制や販売手順を公開できないのでしょうか。
おそらく上の記事のような形となるのでしょうが、ただ意見募集をするのではなく、想定される場面での対応方法などについて、パブコメでしっかり示すべきだと思います。
8月に要指導医薬品として告示を予定しているそうです。
早ければ年内にも発売開始となるかもしれません。
9月18日開催の審議会の議事録がアップされました
【厚労省2025.09.18開催】
要指導・一般用医薬品部会 議事録
https://mhlw.go.jp/stf/newpage_71892.html
何歳以上とするか、腎機能低下者(おそらく販売できない)、販売錠数をどうするかなどの議論が興味深い